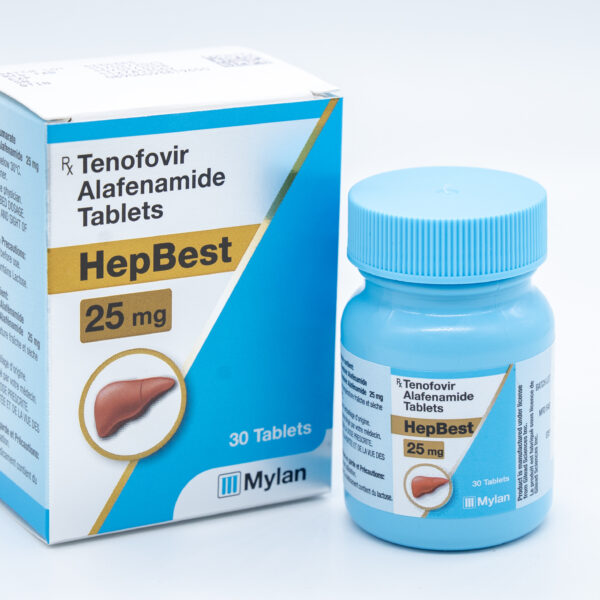
HEPBEST
Danh mục:
Viêm gan B
Quy cách:
Hộp 30 viên
Xuất xứ:
Ấn Độ
Thành phần dược chất:
Tenofovir alafenamide furamate tương đương Tenofovir alafenamide 25 mg
- CHỈ ĐỊNH
Tenofovir alafenamide 25 mg được chỉ định điều trị gan siêu vi B mạn tính ở người lớn và thanh thiếu niên (từ 12 tuổi trở lên có cân nặng có ít nhất 35 kg).
2. LIỀU LƯỢNG VÀ CÁC SỬ DỤNG
Điều trị bằng Hepbest nên được bắt đầu bởi một bác sĩ có kinh nghiệm trong việc điều trị viêm gan B mạn tính
a. Liều lượng:
Người lớn và thanh thiếu niên (từ 12 tuổi trở lên có cân nặng ít nhất 35 kg); một viên mỗi ngày.
b. Ngừng điều trị
- Ngừng điều trị có thể được xem xét dưới đây:
Trong những bệnh nhân dương tính với HBeAg không có xơ gan,điều trị nên được tiến hành ít nhất 6- 12 tháng sau khi chuyển đổi kết quả uyết thanh HBe (HbeAg và HBV DNA biến mất với sự phát triển kháng – HBe) được ác nhận hoặc cho đến khi sự chuyển đổi kết quả huyết thanh HBs hoặc cho điến khi mất hiệu quả. Khuyến cáo đánh giá lại thường xuyên sau khi ngừng điều trị phát triển lại sự tái phát về virus.
Trong những bệnh nhân âm tính với HBeAg không có xơ gan, điuề trị nên được tiến hành ít nhất cho điến hi sự chuyển đổi kết quả huyết thanh HBs hoặc cho đến khi có dấu hiệu mất hiệu quả. Với điều trị kéo dài hơn 2 năm, khuyến cáo đánh giá lại thường xuyên để xác nhậnrằng tiếp tục lựa chọn liệu pháp vẫn còn thích hợp cho bệnh nhân.
- Quên liều
Nếu quên liều và ít hơn 18 giờ trôi qya kể từ thời điểm dùng thuốc thông thường, bệnh nhân nên dùng tenofovir alafenamde sớm nhất chó thể và sau đó tiếp tục dùng liều như kế hoạch bình thường. Nếu quá 18 giờ trôi qua kể từ khi dùng thuốc, bệnh nhân không nên sử dụng liều đã quên và chỉ cần đơn gian nối lại lịch trình dùng bình thường.
Nếu bệnh nhân nôn mửa trong vòng 1 giờ sau khi sử dụng tenofovir alafenamide, bệnh nhân nên dùng một viên thuốc khác. Nếu bệnh nhân nôn mửa sau 1 giờ sử dụng tenofovir aladenamide, bệnh nhân không cần phải uống thêm một viên thuốc nữa.
Dân số đặc biệt
Người cao tuổi
Không điều chỉnh liều của tenofovir alafenamide được yêu cầu trong các bệnh nhân từ 65 tuổi trở lên
Suy thận
Không yêu cầu điều chỉnh tenofovir alafenamide trong bệnh nhân người lớn hoặc thanh thiếu niên (12 tuổi trở lên và cân nặng ít nhất 35 kg) với độ thanh thải creatitine ước tính (CrCl) ≥ 15 mL/phút hoặc trong các bệnh nhân có CrCl < 15mL/phút mà đang chạy thận nhân tạo.
Vào những ngày chạy thận nhân tạo, tenofovir alafenamide nên được dùng sau khi hoàn tất chạy thận nhân tạo.
Không có khuyên cao về liều lượng đối với những bệnh nhân có CrCl < 15mL/phút mà không được chạy thận nhân tạo.
Suy gan
Không điều chỉnh liều của tenofovir alafenamide được yêu cầu ở bệnh nhân suy gan.
Trẻ em
Sự an toàn và hiệu quả của tenofovir alafenamide ở trẻ em dưới 12 tuổi, hoặc cân nặng < 35 kg, chưa được thiết lập. Không có dữ liệu có sẵn.
3. CÁCH DÙNG
Dùng đường uống, Viên nén bao phim tenofovir alafenamide nên được sử dụng với thức ăn
4. CHỐNG CHỈ ĐỊNH
Quá mẫn với bất kỳ thành phần cùng thuốc
5. CẢNH BÁO VÀ THẬN TRỌNG KHI DÙNG THUỐC
Truyền nhiễm HBV
Bệnh nhân phải được thông báo rằng viên nén tenofovir alafenamide không ngăn ngừa được cơ lây truyền HBV sang người khác thông qua quan hệ tình dục hoặc đường máu. Phải tiếp tục sử dụng các biện pháp phòng ngừa thích hợp.
Các bệnh nhân bị bệnh gan mất bù
Không có dữ liệu an toàn và hiệu quả của viên nén tenofovir alafenamide ở những bệnh nhân nhiễm HBV có bệnh gan mất bù và có điểm số Child Pugh Turcotte (CPT)>9 (nghĩa là cấp C). Những bệnh nhân này có nguy cơ cao bị tác dụng không mong muốn nghiêm trọng lên gan và thận. Vì vạy, các thông số về gan mật và thận nên được theo dõi chặt chẽ trong nhóm bệnh nhân này.
Sự trầm trọng hơn của viêm gan
Bùng phát trong điều trị
Sự gia tăng tự phát trong viêm gan B mạn tính là tương đối phổ biến và được đặc trưng bỏi sự gia tăng thoáng qua alanine aminotransferase (ALT) trong huyết thanh. Sau khi bắt đầu điều trị bằng thuốc kháng virus, ALT huyết thanh có thể tăng trong một vài bệnh nhân. Trong các bệnh nhân có bệnh gan còn bù,sự gia tăng ALT huyết thanh nói chung không đi kèm với tăng nồng độ bilirubin huyết thanh hoặc sự mất bù gan. Các bệnh nhân xơ gan có nguy cơ can hơn sự mất bù gan sau khi viêm gan trầm trọng hơn, và vị vậy nên được theo dõi chặt chẽ trong quá trình điều trị.
Bùng phát sau khi ngừng điều trị
Đợt kịch phát cấp của viêm gan đã được báo cáo ở các bệnh nhân đã ngừng điều trị viêm gan B, thường liên quan đến sự tăng nồng độ HBV DNA trong huyết tương. Phần lớn các trường hợp là tự giới hạn bản thân nhưng kịch phát nghiêm trọng, bao gồm cả từ vong, có thể xảy ra sau khi ngừng điều trị viêm gan B. Chức năng gan phải được theo dõi trong khoảng thời gian lặp lại với cả lâm sàng và xét nghiệm trong ít nhất 6 tháng sau khi ngưng điều trị viêm gan B. Nếu thích hợp, việc tiếp tục viêm gan B có thể được bảo đảm.
Trong các bệnh nhân bị bệnh gan tiến triển hoặc xơ gan, ngưng điều trị không được khuyến sau đợt điều trị kích phát của viêm gan có thể dẫn đến sự mất bù của gan. Sự bùng phát của gan đặc biệt nghiêm trọng, và đôi khi gây tử vong ở bệnh nhân bị bệnh gan mất bù.
Hãy là người đầu tiên nhận xét “HEPBEST” Hủy
Sản phẩm tương tự
Viêm gan C
Viêm gan B
Viêm gan B
Ký sinh trùng
Ấn độ
Viêm gan B
Ruột kích thích
Danh mục thuốc















Đánh giá
Chưa có đánh giá nào.